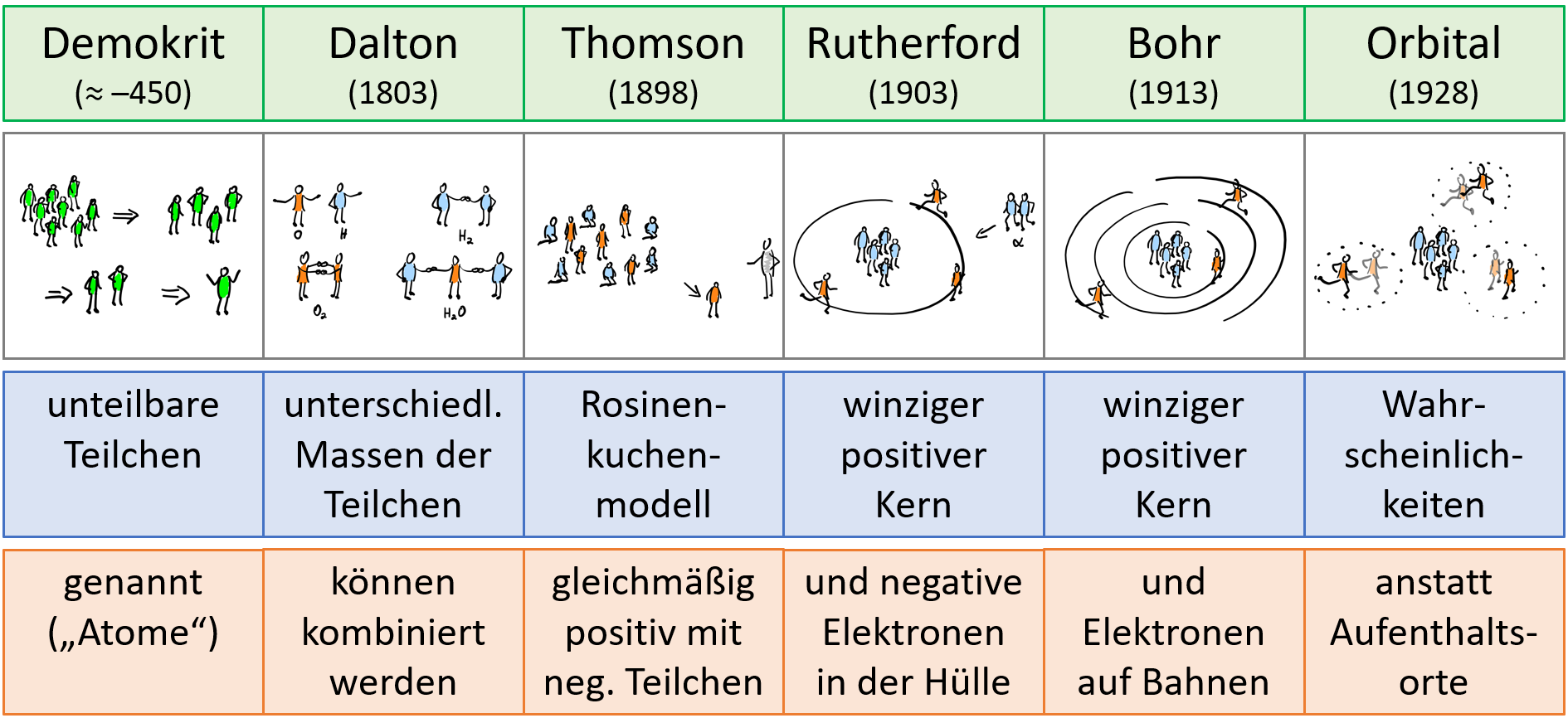
Entwicklung der Atommodelle
Nach dem Modell von Rutherford besteht ein Atom aus einer Hülle und einem Kern. In der fast leeren Hülle befinden sich die negativen Ladungen (leichte Elektronen) und im winzigen Kern positive Ladungen (schwere Protonen) und neutrale Teilchen (schwere Neutronen). Die Kernkraft hält die Protonen und Neutronen im Kern zusammen.
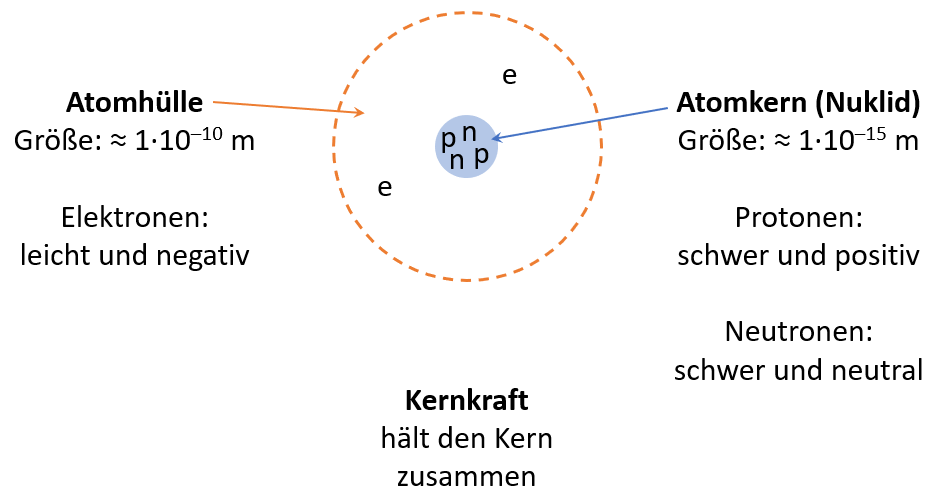
Eine Million Atome ergeben aneinandergereiht ca. 0,1 mm.
Der Kern macht weniger als 0,00001% der Größe aus. In ihm befindet sich aber über 99,9% der Masse.
Die Zusammensetzung von Atomen und die dazugehörige Symbolschreibweise soll mit der folgenden Simulation und den Aufgaben verstanden werden.
Öffne die Simulation Bau ein Atom – PhET und starte dort die mittlere: "Symbol". Lege das Periodensystem und eine Nuklidkarte bereit (Z.B: Buch S. 248 & 250).
Probiere ein wenig darin herum. Du kannst Protonen oder Neutronen in den Kern oder Elektronen in die Hülle ziehen. Ebenso kannst du sie wieder herausziehen oder mit dem orangenen Kreispfeil wieder alles auf 0 setzen. Rechts wird dir das gebaute Atom als Symbol angezeigt.
In der Simulation wird jeweils das Symbol und daran oben rechts zusätzlich die elektrische Ladungszahl angezeigt.
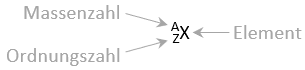
Ziehe einige Protonen, Neutronen und Elektronen in das Atom und achte darauf, was sich jeweils am Symbol verändert.
a) Wodurch wird das Element bestimmt?
b) Was gibt jeweils die Ordnungszahl und die Massenzahl an?
c) Wodurch kann die Ladungszahl auf 0, +1 und -1 gebracht werden?
Baue ein Atom mit 10 Protonen, 10 Neutronen und 9 Elektronen.
a) Welches Element ergibt das?
b) Beschreibe, wie du anhand der Teilchen-Anzahlen und dem Periodensystem das Element bestimmen kannst.
c) Ist es elektrisch positiv, negativ oder neutral geladen? Wie kann man das schon an den Teilchen-Anzahlen erkennen?
Baue folgendes Atom: \(^{\textnormal{13}}_{\textnormal{6}}\)C+2
a) Wie groß ist die Anzahl der Neutronen und wie berechnet man diese Anzahl am Symbol?
b) Wie viele Elektronen hat das Atom und wie berechnet man deren Anzahl?
c) Gib ein Atom mit gleicher Ordnungszahl, aber einer um 1 höheren Massenzahl an.
d) Gib ein Atom mit gleicher Massenzahl, aber einer um 1 höheren Ordnungszahl an.
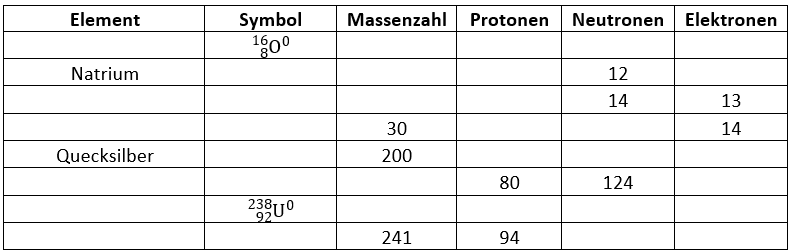
Ergänze die Tabelle. Die Atome sollen jeweils elektrisch neutral (Ladungszahl = 0) sein.
Ab jetzt unterscheiden wir zwischen Atom und Nuklid. Nuklid bezeichnet nur den Aufbau des Atomkerns. Die Elektronen in der Hülle sind dafür unwichtig.
Gib für die folgenden Nuklide jeweils an, wie viele Protonen und Neutronen sie enthalten. Gib dann auch an, um welches Element es sich jeweils handelt.
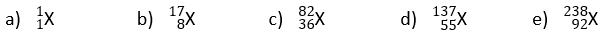
Wasserstoff kommt in drei Nukliden vor. Mit Deuterium und Tritium versucht man Fusionsreaktoren zu bauen, die eine sichere Atomenergie-Quelle wären. Gib jeweils die Symbol-schreibweise an.
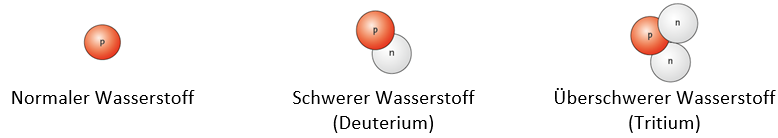
Ein weiterer Begriff zur Beschreibung von Atomen und Kernen ist „Isotop“. Die drei Nuklide des Wasserstoffs unterschieden sich nicht im Element, sondern nur in der Neutronen-Anzahl. Es sind drei Isotope des Elements Wasserstoff.
Baue folgendes Nuklid: \(^{\textnormal{16}}_{\textnormal{8}}\)O
Aktiviere unten rechts den Haken bei „Zeige Stabil / Instabil“. Füge dann mehrere Neutronen hinzu. Nimm danach viele Neutronen weg. Du hast damit verschiedene Isotope von Sauerstoff gebaut.
a) Für welche Massezahlen sind die Isotope stabil?
b) Woran erkennt man das in der Nuklidkarte?
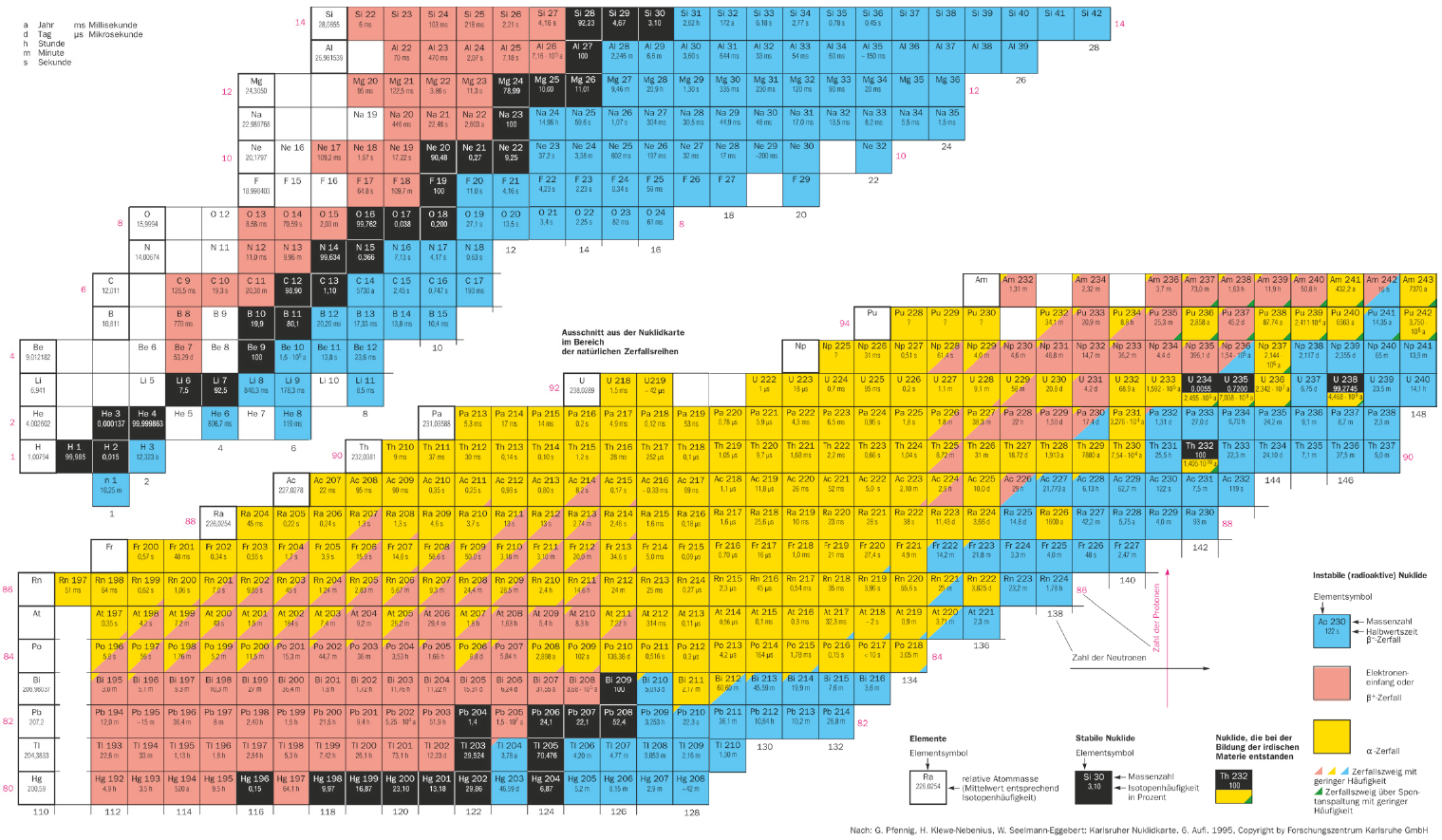
Hier ist ein Ausschnitt der Nuklidkarte abgebildet:
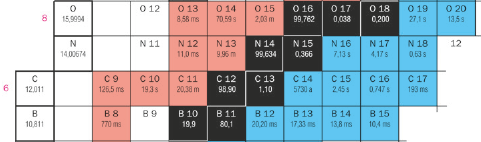
a) Gib die Elemente an, die dort angeführt sind.
b) Gib die Nuklid-Symbolschreibweise für folgende Isotope an: O-16, N-14, N-15, C-12 und B-11.
Stabile Isotope sind in der Nuklidkarte (z.B. auf S. 250) schwarz gefärbt.
a) Wie findet man in der Nuklidkarte die stabilen Isotope von Magnesium (Mg)?
b) Wo steht dort die Protonen-Anzahl (Ordnungszahl) von Magnesium?
c) Wie viele Neutronen haben die Isotope Mg-24, Mg-25 und Mg-26?
Beschreibe ausführlich, wie die Begriffe Atom, Nuklid und Isotop zusammenhängen.
Atom
Die Gesamtheit der Teilchen: Elektronen in der Hülle und Protonen und Neutronen im Kern. Die elektrische Ladung eines Atoms ergibt sich aus: Anzahl Protonen Minus Anzahl Elektronen.
Z.B. 3 Protonen - 4 Elektronen = -1
Nuklid = Atomkern
Der Kern besteht aus Protonen und Neutronen. Die Anzahl der Protonen bestimmt das Element (und damit die chemischen Eigenschaften). Die Neutronen tragen zur Masse und Stabilität des Atoms bei. Zu wenige oder zu viele Neutronen können zu radioaktiver Strahlung durch Kernzerfall führen.
Ein Nuklid kann leicht mit der Symbolschreibweise angegeben werden: \(^{\textnormal{A}}_{\textnormal{Z}}\)X
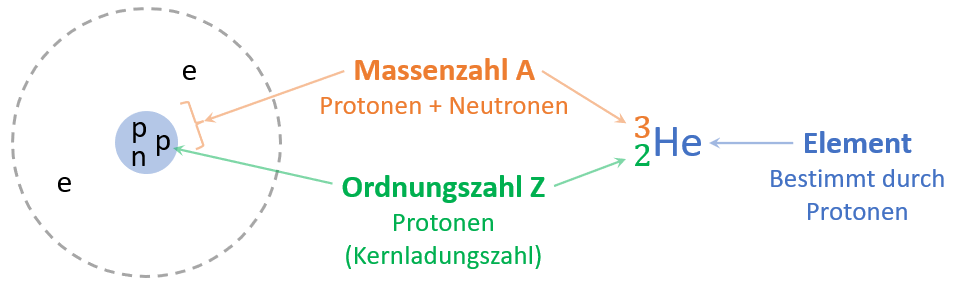
Isotop
Atomkerne eines gleichen Elements können unterschiedlich viele Neutronen haben. Man nennt sie dann Isotope des Elements. In der Nuklidkarte sind alle möglichen Nuklide aufgeführt. Links steht das jeweilige Element und in der Zeile befinden sich alle Isotope. Die Protonen-Anzahl wird nach oben erhöht und die Neutronen-Anzahl nach links. (Die schwarzen sind stabil und die farbigen zerfallen.)
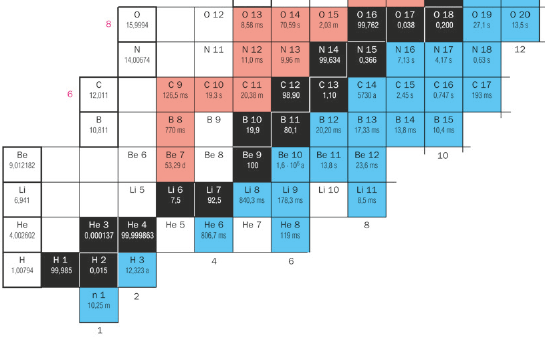
Beispiel: B-11 ist ein stabiles Bor-Isotop mit 5 Protonen und 6 Neutronen. B-12 ist instabil mit 5 Protonen und 7 Neutronen.
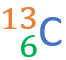
6 Protonen (zu sehen an der Ordnungszahl 6)
Element Kohlenstoff (aufgrund der 6 Protonen)
7 Neutronen (Massenzahl Minus Ordnungszahl)
6 Elektronen (wie Protonen-Anzahl, sofern elektrisch neutral)
Geschrieben als Kohlenstoff-Isotop: C-13
Es gibt unsichtbare Strahlung, die Atome ionisieren kann. Das heißt, es werden Elektronen aus der Hülle entfernt oder welche hinzugefügt, so dass das Atom nicht mehr elektrisch neutral ist. Dadurch wird z.B. Luft elektrisch leitend. Für Lebewesen ist das gefährlich, weil Zellen (z.B. DNA) dadurch beschädigt werden.
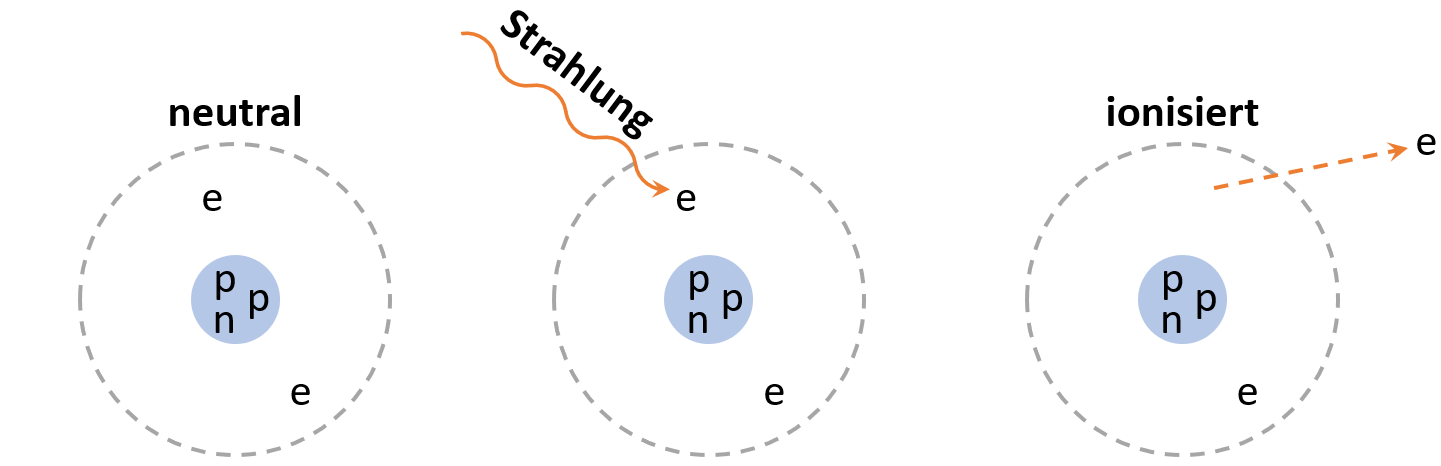
Es werden drei verschiedene Arten der Strahlung unterschieden: α, β und γ
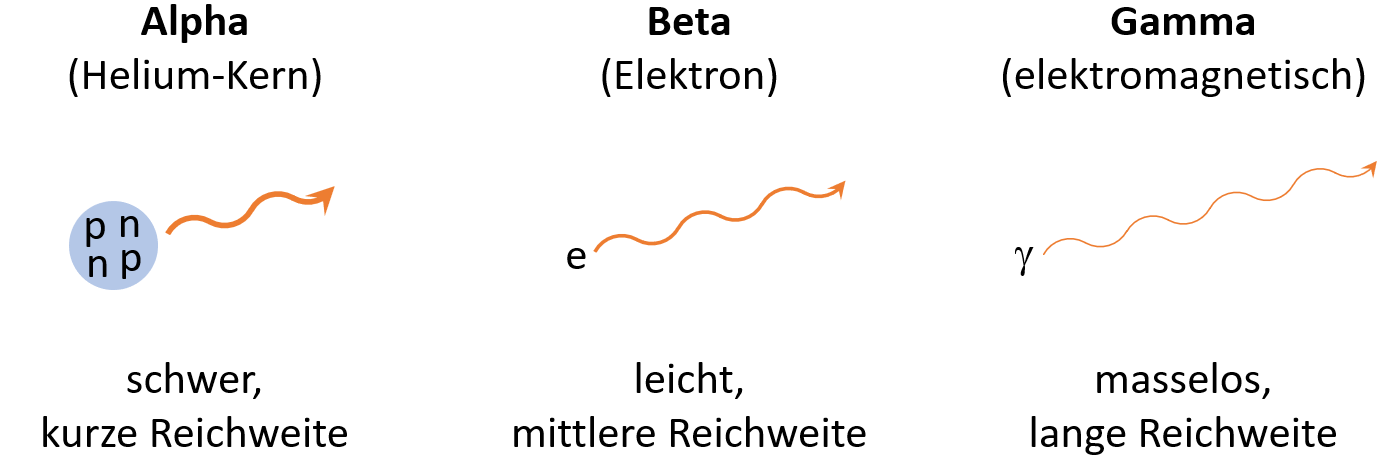
Alpha-Strahlung: Kurze, dicke Nebelspuren
Beta-Strahlung: Lange, dünne Nebelspuren
Gamma-Strahlung: Kaum sichtbar. Manchmal kleine Schnörkel

Mithilfe des Arbeitsblattes und eines Würfels wird das unterschiedliche Durchdringungsvermögen der Strahlungsarten untersucht. Auf dem Arbeitsblatt ist für jede Strahlungsart Kasten mit mehreren Zeilen und grauen Balken zu sehen. Die grauen Balken stellen Materieschichten dar (z.B. Papierblätter). Jede Zeile steht für ein Teilchen der Strahlung, dass diese Schichten zu durchdringen versucht. Es sind 24 Teilchen für jede Strahlungsart.
Würfel für jedes Teilchen und entscheide anhand der folgenden Darstellung, ob es eine Schicht durchdringt bzw. wie viel Energie es dabei verbraucht. Ein Teilchen, dass keine Energie mehr hat, verschwindet. Gamma-Strahlung kann nur existieren oder nicht, ohne andere Energien zu haben.
Die erste Zeile ist für jede Strahlungsart schon ausgefüllt. Beim ersten Alpha-Teilchen wurde zuerst eine 1 gewürfelt. Damit hat es 20 Energie verloren und damit noch 80. Danach wurde eine 3 gewürfelt. Damit hat es 60 Energie verloren und damit noch 20. Dann wurde eine 2 gewürfelt. Es verschwindet nun, da es keine Energie mehr hat.

Arbeitsblatt: Strahlung_durch_Materie.pdf
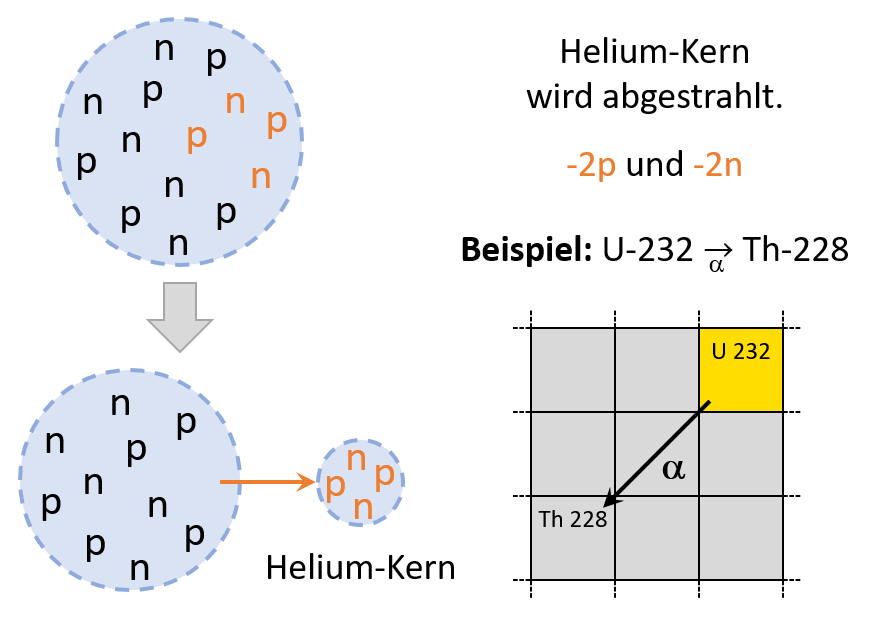
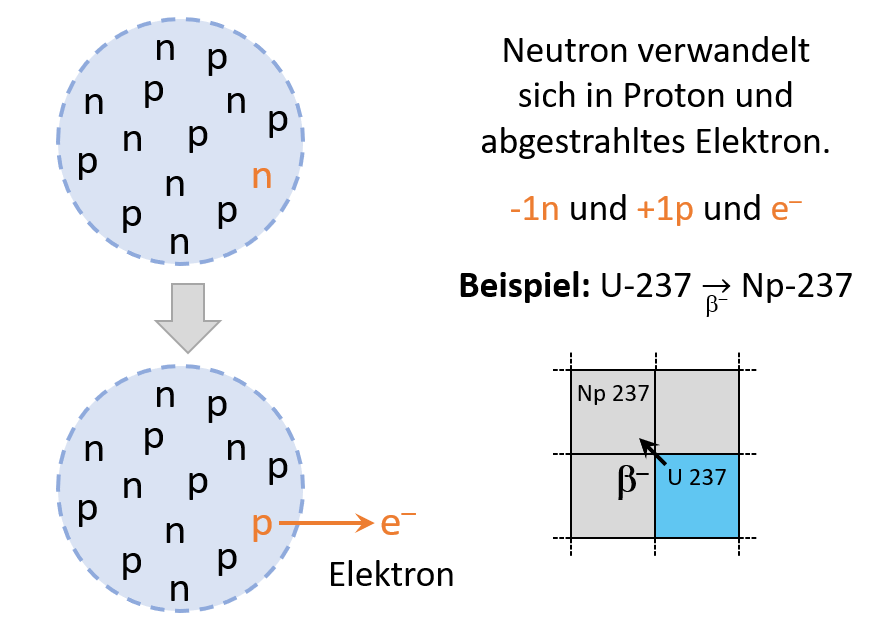
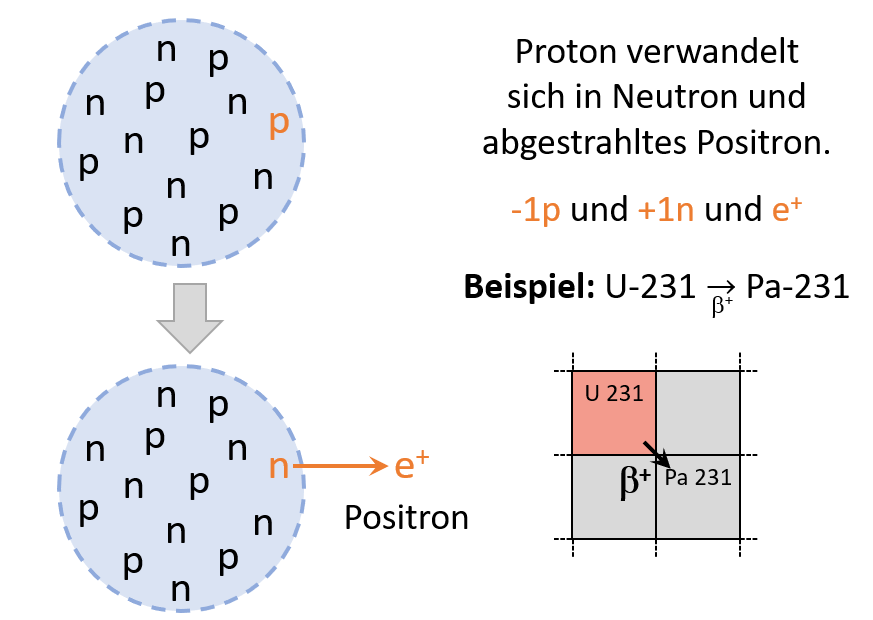
folgen
Welche der folgenden Aussagen sind richtig?
a) Atome sind die kleinsten Teilchen. Deshalb auch der Name von „átomos“ = „unteilbar“.
b) Jedes Atom besitzt einen sehr kleinen Atomkern.
c) Im Atomkern befinden sich die Protonen, Neutronen und Elektronen.
d) Der Atomkern ist elektrisch negativ und die Atomhülle elektrisch positiv geladen.
e) Man nennt das Atommodell auch „Rosinenkuchen“.
f) Ein elektrisch neutrales Atom hat genauso viele Elektronen wie Neutronen.
g) Protonen haben eine positive elektrische Ladung.
h) Elektronen sind viel leichter als Neutronen.
i) Alpha-Strahlung ist viel leichter als Beta-Strahlung.
Was ist ein Element? Was ist ein Isotop? Und was ist ein Nuklid? Beschreibe jeweils kurz.
Gib die richtigen Aussagen an. Zwei Nuklide bezeichnet man als Isotope eines Elements, wenn sie die folgenden Eigenschaften aufweisen:
a) Gleiche Anzahl an Protonen, verschiedene Anzahl an Neutronen.
b) Gleiche Anzahl an Neutronen, verschiedene Anzahl an Protonen.
c) Gleiche Masse der Atomkerne.
d) Gleiche Massezahl und gleiche Elektronenzahl.
e) Verschiedene Massezahl und gleiche Ordnungszahlzahl.
Welche Aussage kann man anhand der Schreibweise 8035Br über das Atom machen? Woran kann man anhand dieser Schreibweise Isotope des Elements erkennen?
Ergänze die fehlenden Angaben zu den Isotopen.
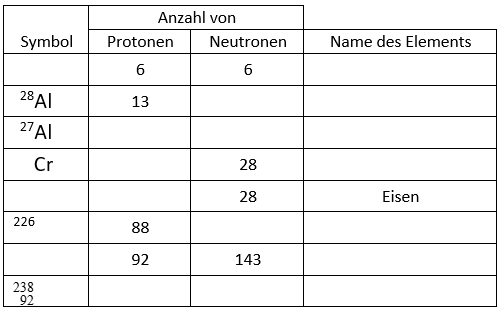
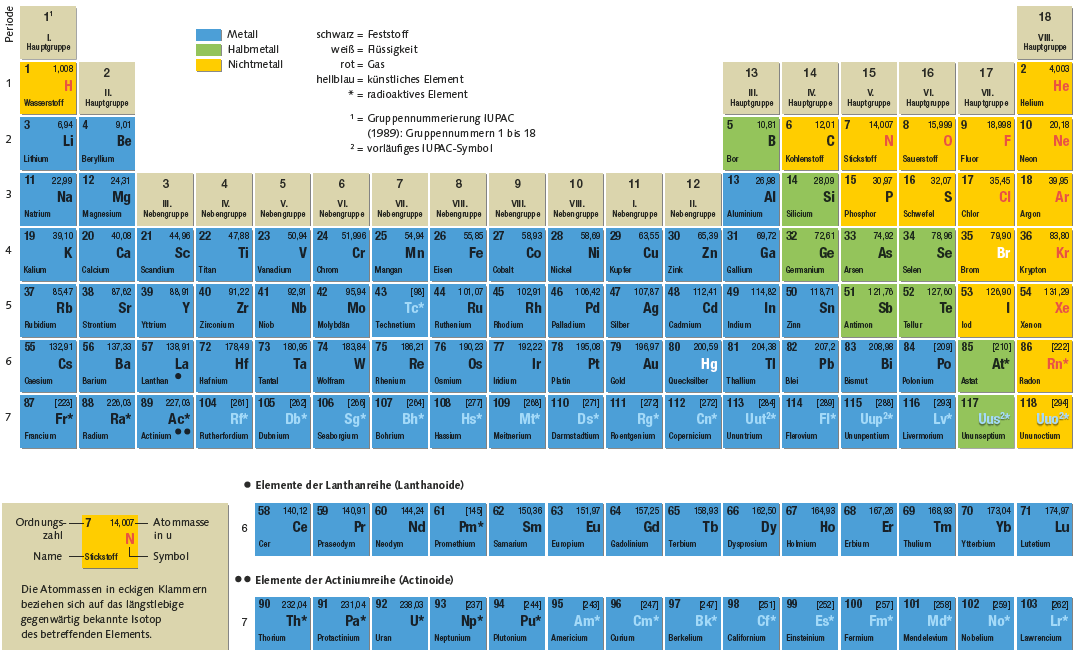
 Im Periodensystem der Elemente findet nur ein Isotop eines Stoffes Platz. Dies ist beispielsweise bei Aluminium das dargestellte Symbol. Am rechten Zahlenwert 26,98 lässt sich ablesen, wie groß die Massezahl ungefähr ist (≈ 27).
Im Periodensystem der Elemente findet nur ein Isotop eines Stoffes Platz. Dies ist beispielsweise bei Aluminium das dargestellte Symbol. Am rechten Zahlenwert 26,98 lässt sich ablesen, wie groß die Massezahl ungefähr ist (≈ 27).
a) Welches Isotop wird allgemein im Periodensystem der Elemente notiert? (Vergleiche Nuklidkarte)
b) Gib die Zahl der Neutronen bei diesem Al-Nuklid des Periodensystems an.
c) Gib das Al-Nuklid in der Bezeichnung Al-"xyz" an, bei dem die Kernladungszahl und die Neutronenzahl beide gleich groß sind.
d) Wie groß ist bei dem gegebenen Al-Nuklid die Zahl der Elektronen, falls es sich um ein elektrisch neutrales Atom handelt?
Nenne mehrere Möglichkeiten, mit denen man Alpha-, Beta- und Gamma-Strahlung unterscheiden kann.
Woran erkennt man die Strahlungsarten in der Nebelkammeraufnahme?

a) Falsch. Ein Atom besteht aus noch kleineren Teilchen.
b) Richtig.
c) Falsch. Die Elektronen befinden sich in der Hülle, nicht im Kern.
d) Falsch. Andersrum.
e) Falsch. Man hat es früher mal so genannt, seit Rutherford aber nicht mehr.
f) Falsch.
g) Richtig.
h) Richtig.
i) Falsch. Andersrum.
Element: Atomart, die durch die Protonenanzahl festgelgt ist.
Isotop: Varianten eines Atomkerns, bei der die Neutronenanzahl unterschiedlich ist.
Nuklid: Anderes Wort für Atomkern eines Elements. Ein Nuklid besteht aus Protonen und Neutronen und kann mit der Symbolschreibweise kompakt notiert werden.
a) Richtig.
b) Falsch. Isotope eines Elements haben immer gleich viele Protonen.
c) Falsch. Durch die unterschiedliche Neutronenanzahl sind sie unterschiedlich schwer.
d) Falsch. Durch die unterschiedliche Neutronenanzahl ist die Massezahl verschieden.
e) Richtig.
Es besteht aus 35 Protonen, 45 Neutronen (80-35) und gehört zum Element Brom.
Isotope erkennt man an der unterschiedlichen Massezahl (z.B. 81). Der Rest bleibt gleich.
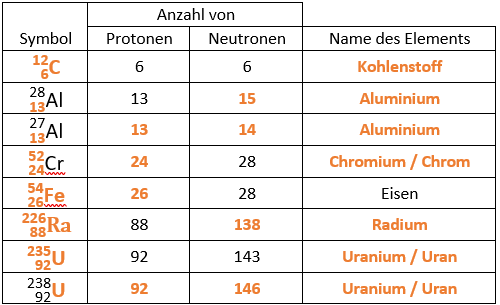
a) Das Isotop, das am häufigsten in der Natur vorkommt.
b) Protonanzahl ist für Aluminium immer 13. Die Neutronenanzahl dieses Isotops ist also 14 (27-13).
c) Al-26
d) 13 (genauso viele wie Protonen)
- An den unterschiedlichen Nebelspuren in einer Nebelkammer.
- Am unterschiedlichen Durchdringungsverhalten durch Materie.
(- An ihrer verschiedenen Ladung: Man kann sie mit einem Magneten unterschiedlich ablenken.)
- Alpha-Strahlung: Kurze, dicke Spuren. Meistens ganz gerade.
- Beta-Strahlung: Lange, dünne Spuren. Meistens mit Knicken oder Kurven.
- Gamma-Strahlung: Kaum zu erkennen. Manchmal kleine Knäuel.
Wir wissen, dass Atome zerfallen können und das dies je nach Element unterschiedlich lange dauern kann. Tatsächlich ist es für ein einzelnes Atom jedoch sehr zufällig, wann es zerfällt. Erst eine große Anzahl solcher Atome führt dazu, dass man aus den Zufällen eine Gesetzmäßigkeit erkennen kann.
Wir simulieren dies wieder durch Würfeln. Ein Würfel symbolisiert ein Atom. Bei einer "6" zerfällt das Atom, ansonsten bleibt es zunächst erhalten. Damit wir eine große Anzahl dieser "Atome" haben, würfelt jeder mit 50 Würfeln und am Ende werden alle Würfe der Klasse zusammengetragen. Nicht-zerfallene "Atome" werden beim nächsten Durchgang nochmals gewürfelt und die zerfallenen herausgenommen. Dies wird so lange gemacht, bis alle "Atome" zerfallen sind bzw. maximal 25 Durchläufe.
Jede(r) wird würfeln und dabei in einer Tabelle notieren, wie oft eine "6" vorkam und wie viele Würfel übrig blieben. Begonnen wird mit insgesamt 50 würfeln (sozusagen 50 Atomen). Die Anzahl der 6en wird beim nächsten Wurf von der Gesamtanzahl abgezogen, so dass es immer weniger Würfel werden. Insgesamt soll es 25-mal durchgeführt werden (außer es sind vorher schon keine Würfel mehr übrig).
| Nummer | 1 | 2 | 3 | 4 | ... |
| Würfel | 50 | 41 | 33 | 28 | ... |
| 6en | 9 | 8 | 5 | 5 | ... |
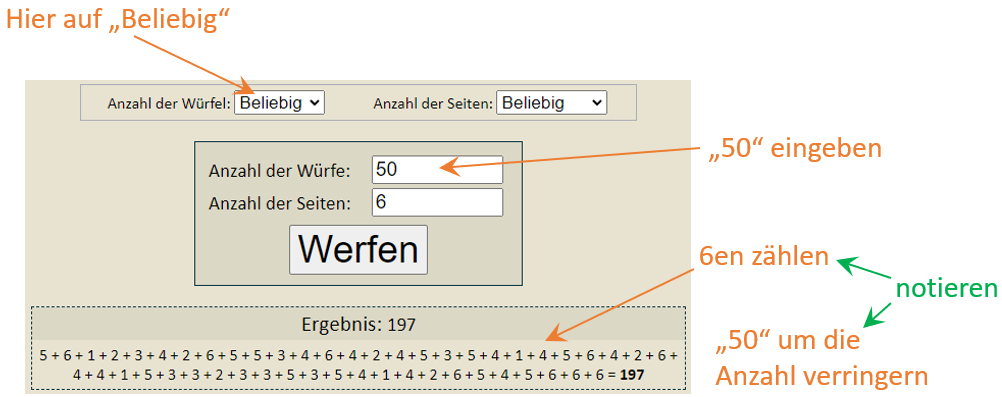
Zum Beispiel mit online-wuerfel.de (Link anklickbar): Dort „Anzahl der Würfel“ auf „Beliebig“ stellen. Dann beginnen mit „Anzahl der Würfe:“ 50 und „Anzahl der Seiten:“ 6
Bei den Ergebnissen müssen dann selbst die 6en gezählt werden. Ihre Anzahl wird notiert und diese wird von der Gesamtanzahl der Würfel abgezogen. Beispiel: Von 50 Würfeln zeigten 9 eine „6“. Dann werden beim nächsten Wurf nur noch 41 Würfel geworfen. Wenn davon 8 eine „6“ zeigen, werden danach nur noch 33 Würfel geworfen. Dafür muss jeweils die neue "Anzahl der Würfe:" eingetragen werden.
1. Tragt die Ergebnisse von allen in einer gemeinsamen Tabelle zusammen (z.B. an der Tafel durch Klassensprecher). Dabei sollen die Zahlen der einzelnen Schüler addiert werden, so dass eine hohe Gesamtanzahl notiert wird.
| Nummer | 1 | 2 | 3 | 4 | ... |
| Anzahl | 1150 | 964 | 804 | 669 | ... |
2. Jede(r) schreibt die Tabelle mit den Gesamtanzahlen ab.
3. Stelle den Verlauf der "Atom"-Anzahlen in einem Diagramm dar. x-Achse: Nummer, y-Achse: Anzahl.
4. Beschreibe den Verlauf mit Worten.
5. Notiere:
a) Nach wie vielen Durchläufen ist noch die Hälfte der anfänglichen "Atome" vorhanden?
b) Wie viele Durchläufe sind es von dort an, bis noch die Hälfte der Hälfte vorhanden ist?
c) Wie viele Durchläufe sind es von dort an, bis noch die Hälfte der Hälfte der Hälfte vorhanden ist?
6. Notiere, was bei 5 auffällt und was "Halbwertszeit" bedeuten könnte. (Hinweis: Halbwert = Hälfte)